la famiglia chimica delle furocumarine: modellistica molecolare per nuovi farmaci anti-infiammatori
aggiornamento Aprile 2023
La correzione della proteina CFTR mutata è l’obiettivo prioritario del trattamento della patologia polmonare dei pazienti affetti da fibrosi cistica. La possibilità che “correttori” e “potenziatori” della CFTR mutata siano in grado di curare contemporaneamente anche la componente infiammatoria cronica polmonare non è confermata e suggerisce la necessità di progettare nuovi farmaci antinfiammatori disegnati ad hoc per la specifica patologia polmonare.
Ha quindi sollevato notevole interesse l’azione multipla della 4,6,4’-trimetilangelicina (TMA), furocumarina a geometria di condensazione angolare, nota per essere un modulatore della proteina CFTR, con triplice attività di correzione, di potenziamento e antinfiammatoria (Tamanini et al, 2011; Marzaro et al, 2013; Favia et al, 2014; Lampronti et al, 2017).
TMA è stata ottenuta da uno screening di piante medicinali della tradizione del Bangladesh, che ha identificato inizialmente il capostipite furocumarinico lineare 5-metossipsoralene (5-MOP) (BOX 1) e successivamente l’analogo angolare TMA (BOX 2).


Durante le fasi iniziali dello studio, alcuni derivati hanno dimostrato di agire come antinfiammatori inibendo l’interazione NF-kB/DNA con il promotore di IL-8/CXCL8, anche a minori concentrazioni rispetto alla TMA di riferimento, e di diminuire in cellule fibrocistiche, come la TMA, l’espressione di IL-8/CXCL8, citochina chemiotattica per i neutrofili, marcatore caratteristico della patologia infettivo-infiammatoria tipica del polmone dei pazienti CF.
L’indagine sulle proprietà di TMA è stata poi estesa ad altre potenziali azioni su CFTR mutata, testando i possibili effetti sulla correzione e potenziamento della proteina con la più comune mutazione F508del CFTR (BOX 3).
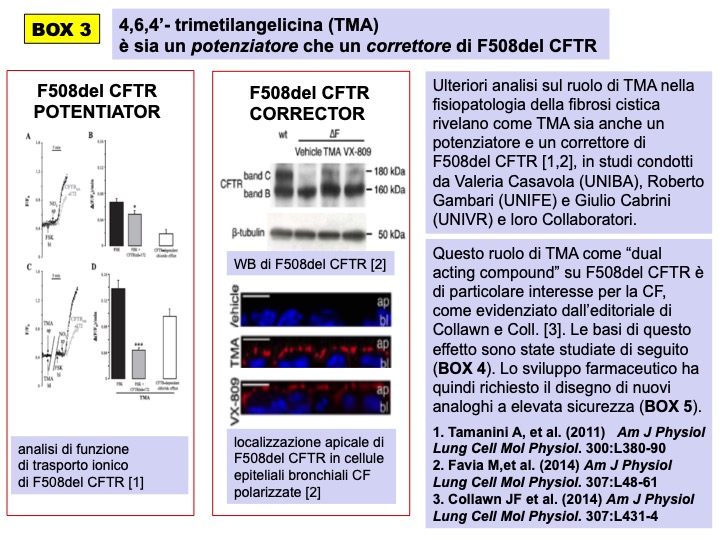
Alcuni di questi derivati hanno mantenuto anche le attività di modulazione di CFTR, ripristinando la funzione in cellule FRT-YFP-F508del, HEK-293 e bronco-epiteliali CF e dimostrando di mediare la correzione attraverso modifica di MSD1 e stabilizzazione indiretta dell’interfaccia tra NBD1 e CL4 (Laselva et al, 2016; Laselva et al, 2018a) (BOX 4).
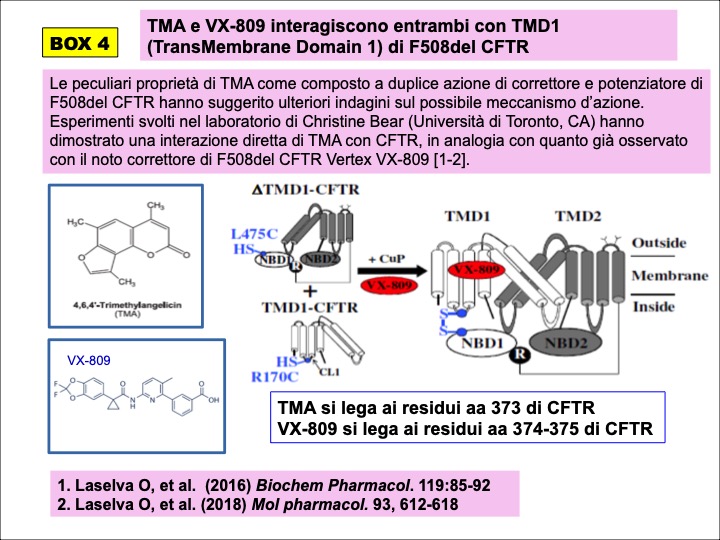
La possibilità di procedere con lo sviluppo industriale farmaceutico di TMA mediante brevettazione internazionale e designazione come Farmaco Orfano della European Medicines Agency è stata valutata grazie a Marco Prosdocimi ed i colleghi Germano Carganico, Fabrizio Minoja e Anita Falezza (Rare Partners, Milano) giungendo alla conclusione che era necessario disegnare nuovi analoghi di TMA ad elevato profilo di sicurezza. Di conseguenza, studi di SAR (relazioni struttura-attività) condotti dal gruppo di Adriana Chilin (UNIPD) hanno permesso di progettare, sintetizzare e selezionare analoghi di TMA completamente privi degli effetti mutageni e fototossici rilevati nella TMA capostipite 4,6,4′-trimetilangelicina, da studiare come possibili correttori e potenziatori di CFTR mutata, nonché come antinfiammatori di nuova generazione, in collaborazione con il gruppo guidato da Ilaria Lampronti (UNIFE) su progetti finanziati dalla Fondazione Italiana per la Ricerca sulla Fibrosi Cistica (BOX 5).
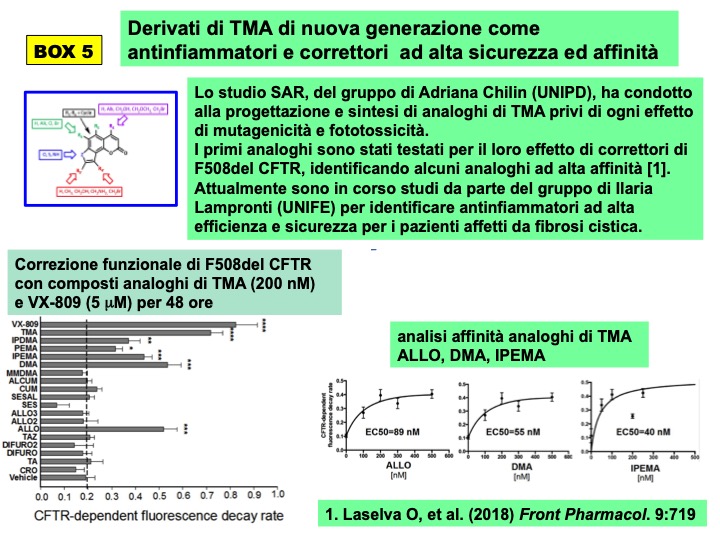
La interazione degli analoghi della TMA con il legame di NF-kB con il sito di consenso nel promotore della chemochina neutrofilica IL-8 (Tamanini et al. 2011; Lampronti et al. 2017) ha indotto una serie di verifiche ulteriori dell’effetto anti-infiammatorio. Analoghi di TMA sono stati sintetizzati dal gruppo collaborativo guidato da Adriana Chilin, portando ad identificare analoghi di TMA privi di fotoreattività, mutagenicitò e tossicità verificata con test in vitro (cfr Vaccarin et al Int J Mol Sci 2022) e a sviluppare da parte dello stesso gruppo formulazioni che implementano la biodisponibilità dopo somministrazione orale in modello murino di questi composti altamente lipofili (cfr Franceschinis et al Pharmaceutics 2022). La libreria di composti selezionata per gli aspetti di sicurezza è quindi stata sottoposta a screening sulla efficacia dell’effetto anti-infiammatorio in modelli sperimentali in vitro ed in modello murino in vivo portando ad identificare l’analogo GY971a come una molecola attiva nel ridurre l’eccessivo richiamo di leucociti neutrofili tipico della patologia polmonare della fibrosi cistica (cfr Tupini at al Int J Mol Sci 2022). Ulteriori studi sono in corso per consolidare i primi risultati ottenuti.
Referenze bibliografiche
Collawn JF, Fu L, Bartoszewski R, Matalon S. Rescuing ΔF508 CFTR with trimethylangelicin, a dual-acting corrector and potentiator. Am J Physiol Lung Cell Mol Physiol. 2014;307:L431-4.
Favia M, Mancini MT, Bezzerri V, Guerra L, Laselva O, Abbattiscianni AC, Debellis L, Reshkin SJ, Gambari R, Cabrini G, Casavola V. Trimethylangelicin promotes the functional rescue of mutant F508del CFTR protein in cystic fibrosi airway cells. Am J Physiol Lung Cell Mol Physiol. 2014;307:L48-61.
Franceschinis, E., Roverso, M., Gabbia, D., De Martin, S., Brusegan, M., Vaccarin, C., Bogialli, S., Chilin, A. (2022) Self-Emulsifying Formulations to Increase the Oral Bioavailability of 4,6,4′-Trimethylangelicin as a Possible Treatment for Cystic Fibrosis. Pharmaceutics 14, 1806
Lampronti I, Manzione MG, Sacchetti G, Ferrari D, Spisani S, Bezzerri V, Finotti A, Borgatti M, Dechecchi MC, Miolo G, Marzaro G, Cabrini G, Gambari R, Chilin A. Differential Effects of Angelicin Analogues on NF-kB Activity and IL-8 Gene Expression in Cystic Fibrosis IB3-1 Cells. Mediators Inflamm. 2017;2017:2389487.
Laselva O, Molinski S, Casavola V, Bear CE. The investigational Cystic Fibrosis drug Trimethylangelicin directly modulates CFTR by stabilizing the first membrane-spanning domain. Biochem Pharmacol. 2016;119:85-92.
Laselva O, Molinski S, Casavola V, Bear CE. Correctors of the Major Cystic Fibrosis Mutant Interact through Membrane-Spanning Domains. Mol Pharmacol. 2018a;93:612-618.
Laselva O, Marzaro G, Vaccarin C, Lampronti I, Tamanini A, Lippi G, Gambari R, Cabrini G, Bear CE, Chilin A, Dechecchi MC. Molecular Mechanism of Action of Trimethylangelicin Derivatives as CFTR Modulators. Front Pharmacol. 2018b;9:719.
Marzaro G, Guiotto A, Borgatti M, Finotti A, Gambari R, Breveglieri G, Chilin A. Psoralen derivatives as inhibitors of NF-κB/DNA interaction: synthesis, molecular modeling, 3D-QSAR, and biological evaluation. J Med Chem. 2013;56:1830-42.
Marzaro G, Lampronti I, D’Aversa E, Sacchetti G, Miolo G, Vaccarin C, Cabrini G, Dechecchi MC, Gambari R, Chilin A. Design, synthesis and biological evaluation of novel trimethylangelicin analogues targeting nuclear factor kB (NF-kB). Eur J Med Chem. 2018;151:285-293.
Nicolis E, Lampronti I, Dechecchi MC, Borgatti M, Tamanini A, Bezzerri V, Bianchi N, Mazzon M, Mancini I, Giri MG, Rizzotti P, Gambari R, Cabrini G. Modulation of expression of IL-8 gene in bronchial epithelial cells by 5-methoxypsoralen. Int Immunopharmacol. 2009;9:1411-22.
Piccagli L, Borgatti M, Nicolis E, Bianchi N, Mancini I, Lampronti I, Vevaldi D, Dall’Acqua F, Cabrini G, Gambari R. Virtual screening against nuclear factorκB (NF-κB) of a focus library: Identification of bioactive furocoumarin derivatives inhibiting NF-κB dependent biological functions involved in cystic fibrosis. Bioorg Med Chem. 2010;18:8341-9.
Tamanini A, Borgatti M, Finotti A, Piccagli L, Bezzerri V, Favia M, Guerra L, Lampronti I, Bianchi N, Dall’Acqua F, Vedaldi D, Salvador A, Fabbri E, Mancini I, Nicolis E, Casavola V, Cabrini G, Gambari R. Trimethylangelicin reduces IL-8 transcription and potentiates CFTR function. Am J Physiol Lung Cell Mol Physiol. 2011;300:L380-90.
Tupini, C., Chilin, A., Rossi, A., De Fino, I., Bragonzi, A., D’Aversa, E., Cosenza, L.C., Vaccarin, C., Sacchetti, G., Borgatti, M., Tamanini, A., Dechecchi, M.C., Sanvito, F., Gambari, R., Cabrini, G., Lampronti, I. (2022) New TMA (4,6,4′-Trimethyl angelicin) Analogues as Anti-Inflammatory Agents in the Treatment of Cystic Fibrosis Lung Disease. Int J Mol Sci. 23, 14483
Vaccarin, C., Gabbia, D., Franceschinis, E., De Martin, S., Roverso, M., Bogialli, S.,Sacchetti, G., Tupini, C., Lampronti, I., Gambari, R., Cabrini, G., Dechecchi, M.C., Tamanini, A., Marzaro, G., Chilin, A. (2022) Improved Trimethylangelicin Analogs for Cystic Fibrosis: Design, Synthesis and Preliminary Screening. Int J Mol Sci. 23, 11528
